美 FDA, 오미크론 백신·치료제 신속 승인 방안 검토
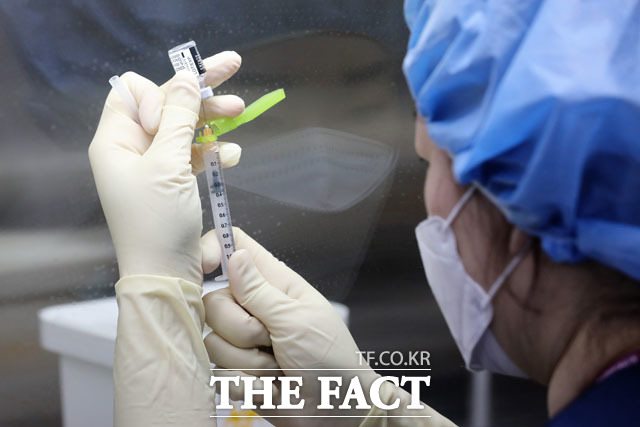
3일(현지시간) 미국 식품의약국(FDA)이 코로나19 신종 변이 바이러스인 오미크론에 대한 백신과 치료제에 대해 신속하게 검토하기 위한 준비를 하고 있다는 현지 보도가 나왔다. /더팩트 DB
WSJ, 3일 소식통 인용 보도…개발 및 테스트에 3개월 전망 [더팩트|원세나 기자] 미국 식품의약국(FDA)이 코로나19 신종 변이 바이러스인 오미크론에 대한 백신과 치료제에 대해 신속하게 검토하기 위한 준비를 하고 있는 것으로 알려졌다.
3일(현지시간) 월스트리트저널(WSJ)은 소식통들을 인용해 FDA가 백신 접종과 치료제 평가를 위해 마련된 규칙을 바탕으로 오미크론 변이를 목표로 하는 제품을 신속 평가하는 데 필요한 연구와 데이터에 대한 지침을 수립하고 있다고 보도했다.
이에 따라 FDA가 수립 중인 새 규정에 따라 오미크론 변이용 백신을 개발하는 제약회사들은 코로나19 부스터샷 승인 때와 비슷한 기준을 충족해야 할 것으로 전망된다.
제약사들은 대규모 장기 임상시험 대신 수백 명 정도의 면역반응만 연구해도 백신 긴급사용 승인을 신청할 수 있을 것으로 보인다.
보도에 따르면 제약회사들이 새 백신을 개발하고 테스트하는 데 약 3개월이 필요할 전망이다. 이후 회사는 신속한 검토 과정을 통해 승인을 요청하고 FDA가 결정을 내리기까지 1~2주가 소요될 것이라고 관계자는 전했다.
제약회사들은 오미크론을 표적으로 하는 백신과 치료제 개발을 위해 이미 움직이고 있다. 화이자의 앨버트 불라 최고경영자(CEO)는 100일 이내 백신을 준비할 수 있다고 밝혔고, 모더나는 임상시험용 백신으로 만드는 데까지 60~90일 정도 걸릴 것이라고 내다 봤다.
- 발로 뛰는 <더팩트>는 24시간 여러분의 제보를 기다립니다.
- · 카카오톡: '더팩트제보' 검색
- · 이메일: jebo@tf.co.kr
- · 뉴스 홈페이지: https://talk.tf.co.kr/bbs/report/write
- · 네이버 메인 더팩트 구독하고 [특종보자→]
- · 그곳이 알고싶냐? [영상보기→]
AD
